Ацетон (acetonum, от латинского acetum — «уксус») — простейший представитель алифатических кетонов.
В норме в небольших количествах ацетон обнаруживается в моче и в крови, у больных сахарным диабетов — в бо́льших концентрациях. Ацетон присутствует среди продуктов сухой перегонки дерева, сахара, целлюлозы и т. п. По этой причине кетоны всегда содержатся в неочищенном метиловом спирте (древесном спирте), откуда значительную часть ацетона можно выделить дробной перегонкой.
Получение ацетона
В больших количествах ацетон получают сухой перегонкой ацетата кальция:
(CH3CO2)2Ca = CaCO3 + CH3COCH3
Сквибб получал ацетон пропусканием паров уксусной кислоты через вращающийся железный цилиндр наполненный смесью пемзы и осаждённого карбоната бария при температуре 500–600° C. Затем смесь паров ацетона, уксусной кислоты и воды подают в конденсирующий аппарат — уксусная кислота и вода остаются в первой части конденсатора, а ацетон — в отдельном сосуде. Карбонат бария служит катализатором — температура, при которой ведётся процесс всегда выше температуры разложения ацетата бария.
Полученный ацетон-сырец может быть очищен получением кристаллического соединения с гидросульфитом натрия, его фильтрацией и перегонкой с карбонатом натрия:
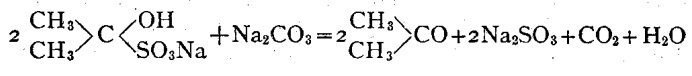
Затем он обезвоживается и перегоняется повторно.
Применение ацетона
Большие количества ацетона идут на приготовление кордита. С этой целью первичный дистиллят перегоняется повторно с серной кислотой, а затем разделяется на фракционируется.
Применяется в производстве хлороформа, Сульфонала, а также как растворитель.
Ацетон применялся при производстве искусственного индиго.
В лаборатории ацетон применяется преимущественно как растворитель (например, камфоры, целлулоида), для мытья посуды, загрязнённой жиром, маслами или смолами. В то же время он удаляет остатки воды и, будучи летучим, ускоряет сушку.
Ацетон можно купить его в любом хозяйственном магазине, торгующем красками и лаками, поскольку его применяют для снятия старого лака и смывания красок.
Простейший лак на ацетоновой основе, хотя очень прочный или стойкий, можно получить в случае необходимости, растворив 30 граммов шеллака в 200 мл ацетона при энергичном перемешивании. Вместо шеллака можно взять канифоль в порошке (и растворяется она быстрее). После того, как шеллак или канифоль разойдётся в ацетоне, к лаку нужно добавить 5–6 мл очищенного скипидара.
Применение ацетона в медицине
В присутствии йода и щелочи ацетон образует йодоформ.
Препарат Спирон — ацетон в смеси с йодидом калия, глицерином и водой — использовался в виде спрея для вдыхания как средство для купирования приступов чихания и астмы. Ацетон применяли для лечения некоторых случаев одышки.
Отравление ацетоном
Ацетон обладает возбуждающим и наркотическим действием на центральную нервную систему, вызывает острые и хронические отравления.
Ацетон может образовываться в организме в результате декарбоксилирования ацетоуксусной кислоты, накапливающейся при нарушении обмена углеводов и жиров, например, при сахарном диабете.
Свойства
Ацетон (диметилкетон) — CH3–CO–CH3 — светлая, подвижная, прозрачная бесцветная жидкость с сильным специфическим запахом, очень летучая и огнеопасная, кипящая при 56,53° C, с удельным весом 0,819 (0–4° C).
Ацетон хорошо смешивается с водой, этиловым спиртом, этиловым эфиром и бензолом.
С фенилгидразином образует гидразон, с гидроксиламином — оксим.
Восстановление амальгамой натрия превращает ацетон в изопропиловый спирт; окисление с хромовой кислотой даёт уксусную кислоту и углекислый газ. С аммиаком ацетон образует ди- и триацетонамины. С синильной кислотой соединяется напрямую, давая нитрил α-оксиизомасляную кислоту.
При реакциях с различными реагентами, такими как гидроксид кальция, гидроксид калия, серная кислота и т. п., ацетон превращается в продукты конденсации, мезитил оксид C6H10O, форон C9H14O и пр.
При перегонке с серной кислотой ацетон превращается в мезитилен C9H12 (симметричный триметилбензол).